ベンゼンは高校化学の芳香族化合物で、定期試験・大学受験・学び直しのどの層にも頻出する重要単元です。
特に多くの人が混乱しやすいのが、置換反応と付加反応の違いです。また、塩素との反応では常温と高温で反応の種類が変わるため、条件整理が非常に重要です。
この記事では、
- ベンゼンは置換反応しやすい
- ハロゲン化・スルホン化・ニトロ化
- 水素付加・塩素付加
- 常温時と高温時の違い
- テストで狙われやすいポイント
をまとめてわかりやすく解説します。
芳香族の反応は「条件で生成物が変わる」ため、独学だと混乱しやすい単元です。
高校化学を体系的に復習したい方は、スタディサプリ のような映像授業で芳香族だけをまとめて確認すると理解が早いです。
ベンゼンは置換反応しやすい
ベンゼンは炭素が六角形に集まって環非常に安定な構造をしています。この安定性を芳香族性といいます。
アルケンの二重結合なら、臭素や水素がすぐ付加して二重結合が切れます。しかしベンゼンで同じことをすると、この安定な芳香族性が失われてしまいます。
そのためベンゼンは、二重結合を壊す付加反応よりも、Hを別の原子や原子団に置き換える置換反応が起こりやすいのです。
この「芳香族性を壊したくない」という考え方が、ベンゼン反応の基本になります。
ベンゼンの置換反応まとめ
ベンゼンの代表的な置換反応は次の3つです。
- ハロゲン化
- スルホン化
- ニトロ化
ハロゲン化
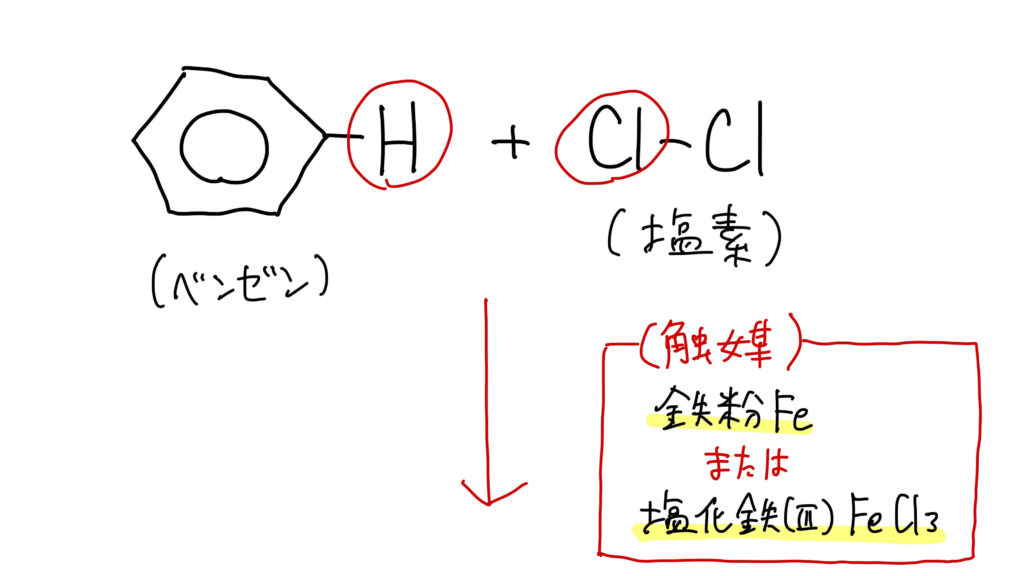
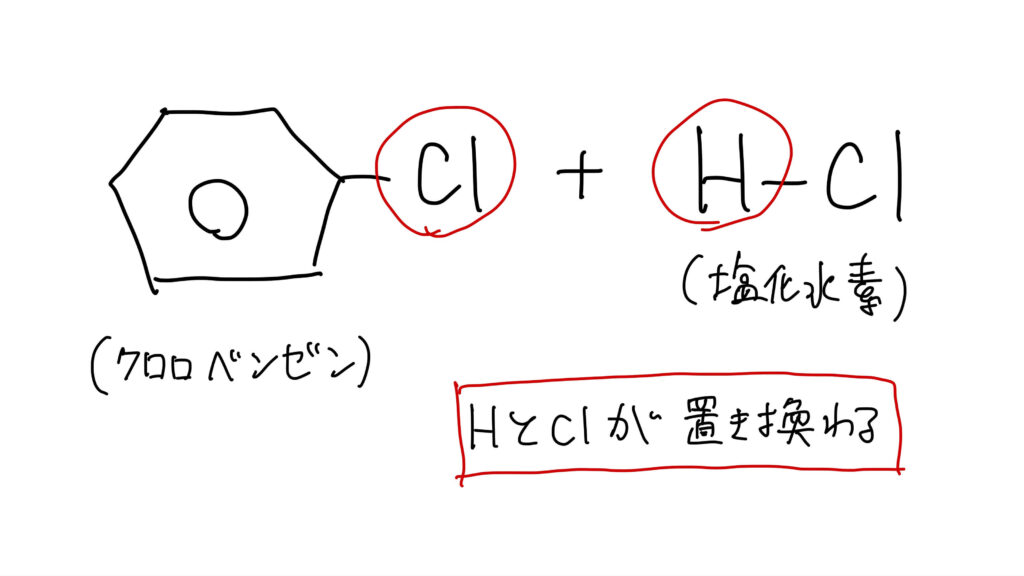
ベンゼンにハロゲン(塩素や臭素)を反応させると、Hがハロゲンに置き換わります。
反応には Fe や FeCl₃ を触媒として用います。
生成物はクロロベンゼンです。
試験では、
- Fe触媒を使う
- 置換反応である
- HがClに変わる
この3点がよく問われます。
スルホン化
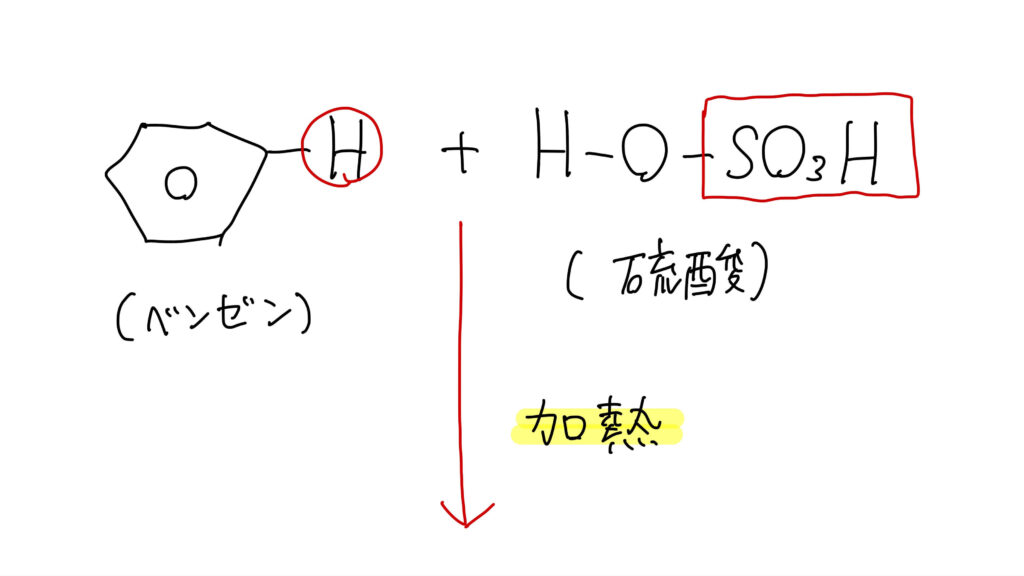
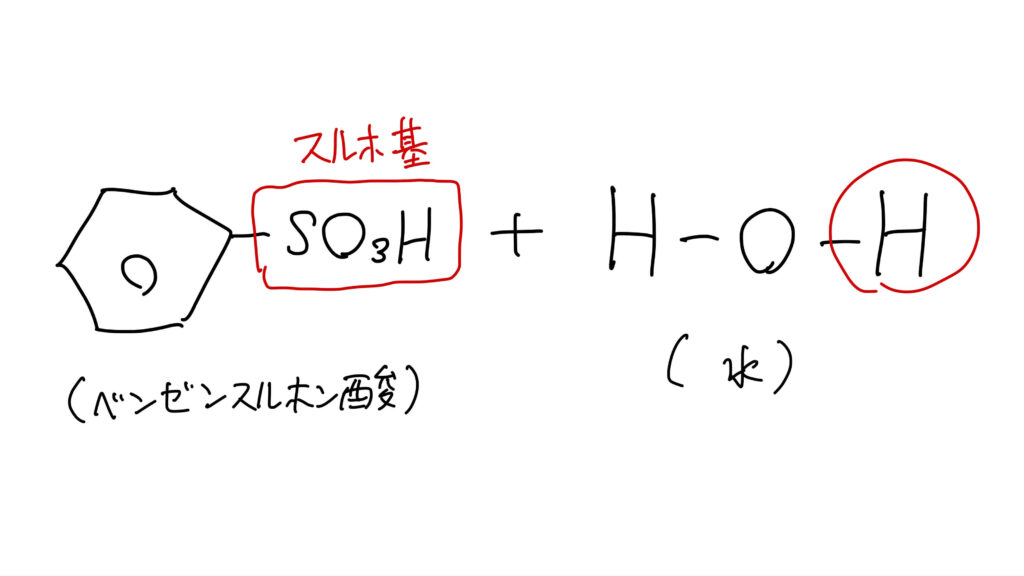
ベンゼンに濃硫酸を反応させると、Hが -SO₃H に置き換わります。
生成物はベンゼンスルホン酸です。
この反応は可逆反応で、条件によって元に戻ることもあります。
共通テストでは単独で深く問われる頻度は高くありませんが、芳香族反応の整理問題で出やすいです。
ニトロ化
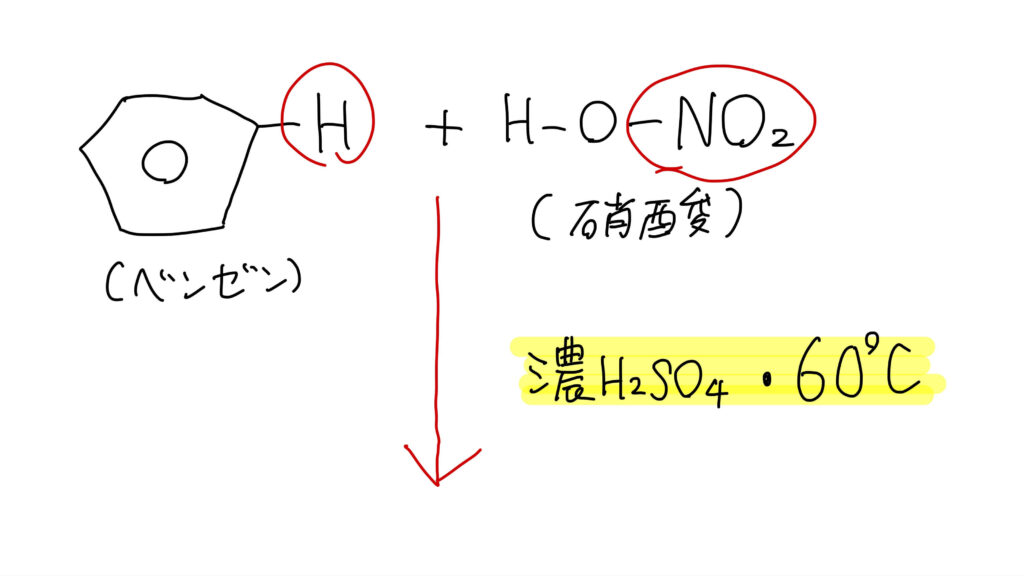
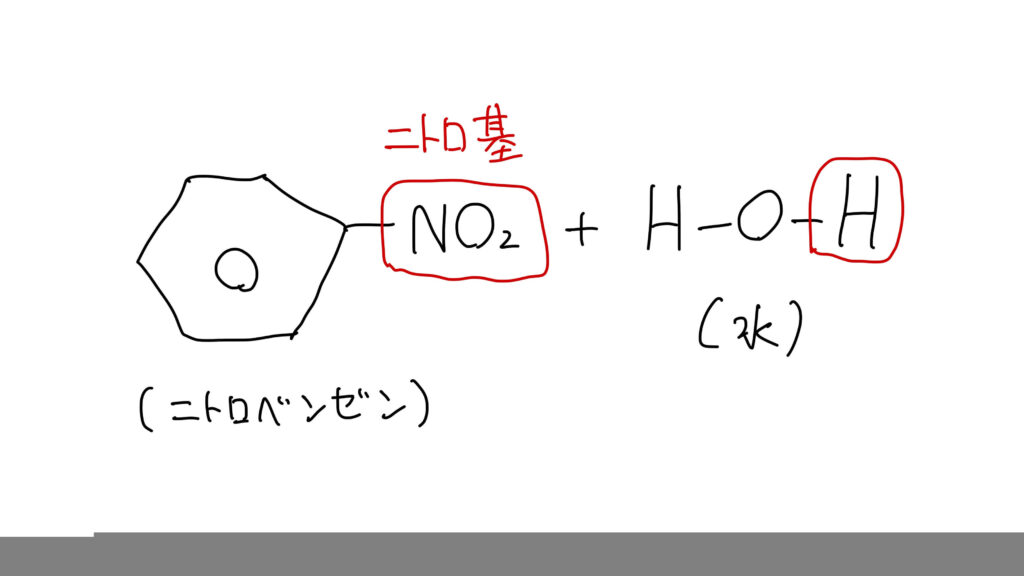
ベンゼンに濃硝酸と濃硫酸の混酸を加えると、Hが -NO₂ に置き換わります。
生成物はニトロベンゼンです。
この反応は非常に重要で、次の
- ニトロベンゼンの還元
- アニリンの生成
- 染料や医薬品の原料
へつながります。
ベンゼンの付加反応まとめ
ベンゼンは基本的には付加しにくいですが、強い条件では付加反応も起こります。
水素H2の付加
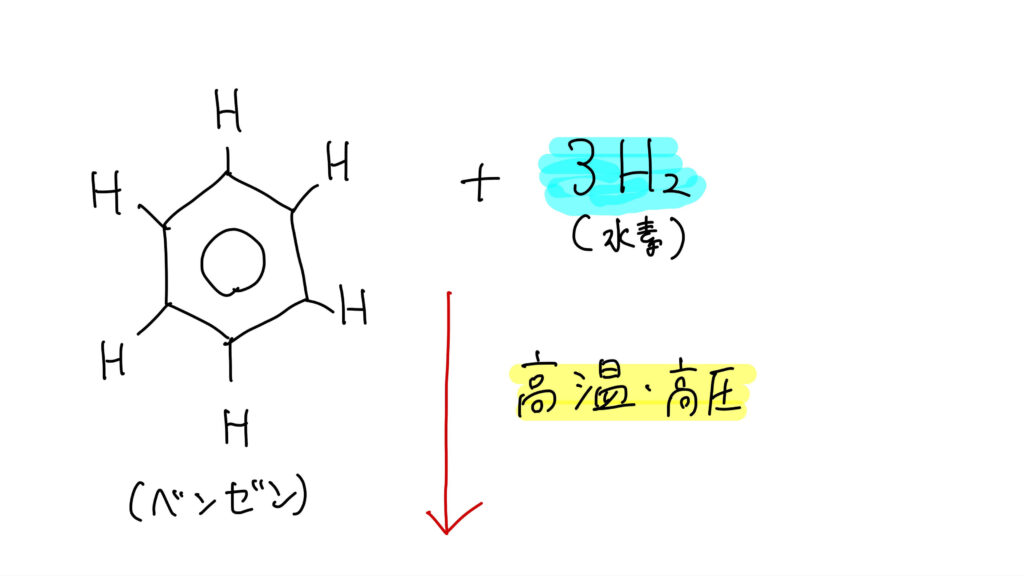
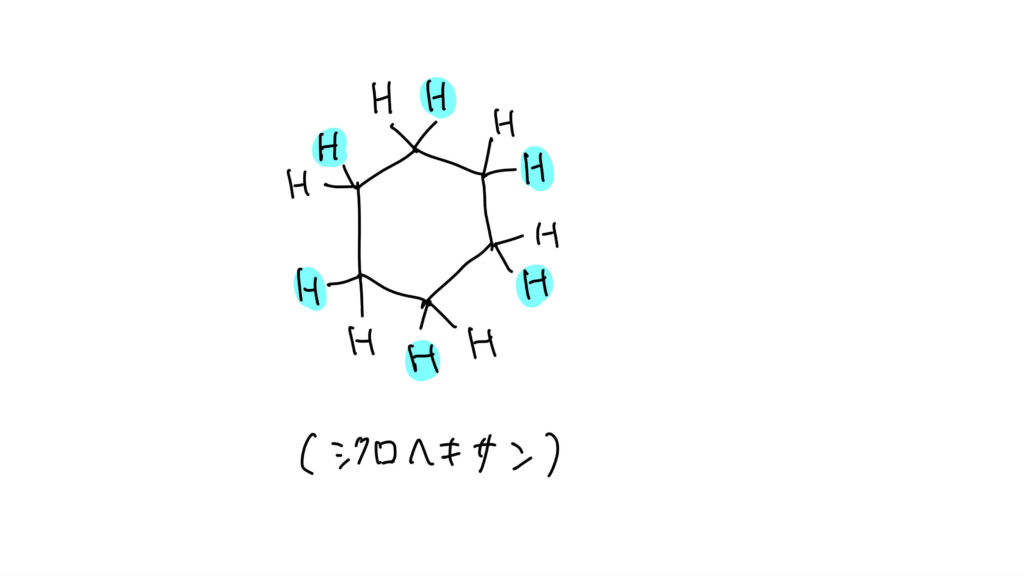
ベンゼンに水素を反応させると、六角形環は残したまま二重結合性が消え、シクロヘキサンになります。
条件は
- ニッケルNiまたは白金Pt触媒
- 高温高圧
です。これは芳香族性を壊すため、強い条件が必要です。
塩素Cl2の付加
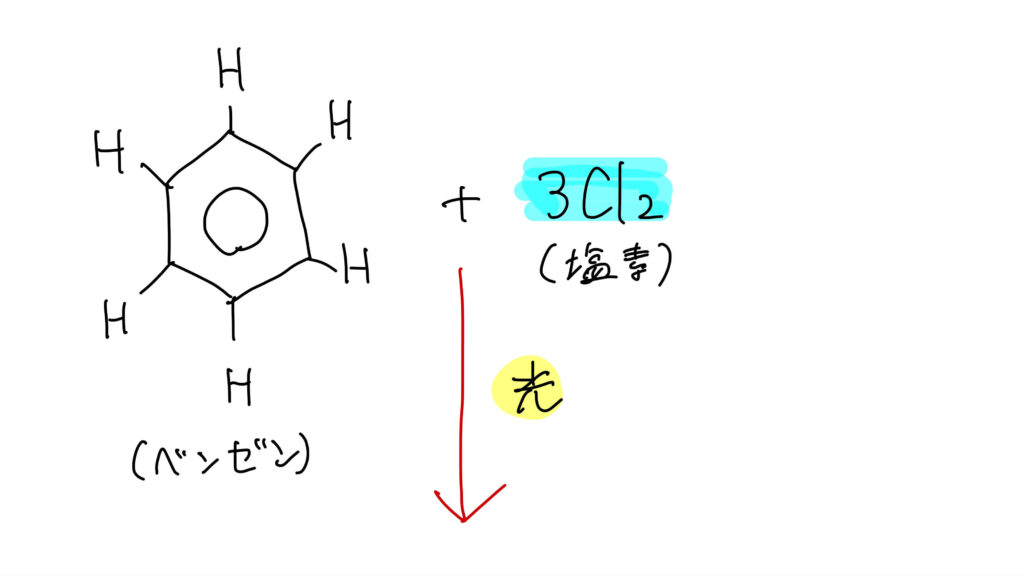
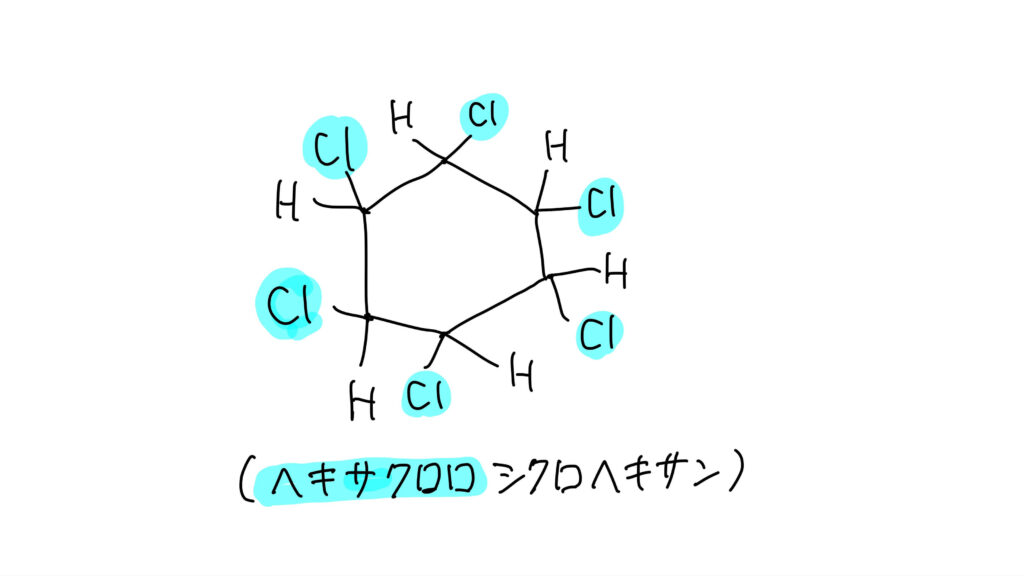
ベンゼンに塩素を反応させ、光を当てると付加反応が起こります。
生成物はヘキサクロロシクロヘキサン(ベンゼンヘキサクロリドBHC)です。
ここは非常に狙われやすいポイントで、
- 光 → 付加
- Fe → 置換
と条件で反応を区別します。
置換反応と付加反応の違いを一発で覚える方法
覚え方はシンプルです。
- 芳香族性を守る → 置換
- 芳香族性を壊す → 付加
この基準で考えると整理しやすくなります。
さらに試験では条件をセットで覚えます。
| 反応 | 条件 | 生成物 |
|---|---|---|
| ハロゲン化 | Fe触媒 | クロロベンゼン |
| スルホン化 | 濃硫酸 | ベンゼンスルホン酸 |
| ニトロ化 | 濃硝酸+濃硫酸 | ニトロベンゼン |
| 水素付加 | Ni・高温高圧 | シクロヘキサン |
| 塩素付加 | 光 | BHC |
この表はそのまま暗記カードにしても効果的です。
まとめ
ベンゼンは二重結合をもつように見えても、芳香族性によって非常に安定です。
そのため基本は付加ではなく置換反応が起こります。
- ハロゲン化(置換)
- スルホン化(置換)
- ニトロ化(置換)
- 水素付加
- 光による塩素付加
この5つを条件とセットで覚えれば、高校化学の芳香族はかなり強くなります。
次はぜひ
「ニトロベンゼンからアニリン」
「フェノールの性質」
までつなげて学習してみてください。
ベンゼンの反応は暗記ではなく「条件比較」で整理すると一気に得点源になります。
化学が苦手な人は、芳香族だけをまとめて復習できる スタディサプリ や化学専門の家庭教師を活用すると、短期間で整理しやすいです。


